Capítulo 3
Avances imagenológicos en urología
- Dr. Andrés Labra W. (1), Dr. Fernando González C.(1), Dra. Daniela Barahona Z. (1), Dr. Carlos Fuentes S.(2)
- (1) Servicio de Radiología, Clínica Alemana – Universidad del Desarrollo
- (2) Servicio de Medicina Nuclear, Clínica Alemana
Introducción
El desarrollo de la urología ha ido de la mano del progreso en la adquisición de imágenes, tanto endoscópicas como radiológicas. La imagenología ha sido y es un campo íntimamente ligado con la patología urológica, tanto desde el punto de vista diagnóstico como del terapéutico.
Desde el descubrimiento de los Rayos X por el profesor Konrad Wilhelm Röntgen en 1895, el progreso y la aplicación de la radiología en la urología ha sido continuo y en constante desarrollo. Un año después J. McIntyre, ya observaba cálculos urinarios mediante rayos X(1).
En las últimas décadas, se ha producido un desarrollo constante en el diagnóstico por imágenes, pasando desde estudios con placas radiográficas simples hasta la introducción de medios de contraste (entre ellos aire) y posteriormente sales iodadas. Es así como comienza la era de la urografía en 1929 cuando Moses Swick descubre que inyectando sales iodadas por vía intravenosa se opacificaba la vía urinaria, lo que permitió una aproximación al estudio de dichas estructuras anatómicas, como también estimar la función renal por unidad renal(2).
Posteriormente el desarrollo de la ecografía (ultrasonografía) cambia totalmente la perspectiva y la manera de abordar al paciente urológico. Se dispone de una técnica no invasiva en tiempo real, con un alto rendimiento diagnóstico y aplicable a embarazadas.
También el desarrollo de la tomografía computada (TC) ha sido un gran paso para la evaluación por imágenes de la patología urinaria. Esta aporta una visión anatómica de los tejidos con una alta sensibilidad y especificidad para el diagnóstico tanto de patología benignas y malignas, pudiendo medirse las unidades “Hounsfield”, de gran importancia para determinar la composición de los tejidos, su impregnación con el contraste intravenoso y densidad de los cálculos.
Una nueva generación de fuentes de imágenes están actualmente al alcance del urólogo: La resonancia magnética (RM) y la tomografía por emisión de positrones por tomografía computada (PET/CT).
La RM es una técnica que no emite radiaciones ionizantes, por lo que es la técnica recomendada en el estudio de la patología genitourinaria en niños y embarazadas, pacientes con falla renal y actualmente en patología prostática y vesical. Presenta mejor resolución de contrastes, no emplea contraste iodado y la utilización del gadolinio es muy útil ya que este presenta muy baja nefrotoxicidad y permite una mejor evaluación de la impregnación de los tejidos y neoplasias.
El PET/CT actualmente es una técnica en constante desarrollo y muy útil para la etapificación de tumores de diversa índole, debido a que permite tanto un estudio anatómico, como funcional de las neoplasias.
La utilización de radionúclidos también ha estado ligada al ejercicio de la urología desde hace años, pudiéndose obtener estimaciones de la función renal por separado, detección de reflujos vésico-ureterales (difícilmente observables por otras técnicas) y la exploración de metástasis óseas a través del cintigrama óseo.
Algunas de estas técnicas han dejado de ser meros métodos diagnósticos, para pasar a ofrecer posibilidades terapéuticas mínimamente invasivas. Gracias a la evolución de las imágenes en los últimos años se ha podido tratar la litiasis de manera no invasiva mediante la litofragmentación renal extracorpórea (LEC), se han desarrollado técnicas percutáneas (nefrolitotomía) y ha cambiado el abordaje de muchas otras patologías, incluidos ciertos tumores(3).
La colaboración del urólogo y del radiólogo es algo fundamental en el momento actual de la medicina, para así ofrecerle al paciente urológico todas las posibilidades diagnósticas y de tratamiento. A continuación se resumen algunas de las características e indicaciones de los estudios de imágenes que nos parecen más relevantes para el urólogo general.
Urolitiasis
La litiasis urinaria es una patología frecuente, en particular en la medicina de urgencia, con prevalencia e incidencia reportadas que han ido en aumento(4). En Chile no se cuenta con datos demográficos confiables. En los Estados Unidos de Norteamérica las personas tienen una probabilidad de 10-15% de presentar un episodio sintomático de litiasis urinaria durante su vida adulta, con un porcentaje de recurrencia de 42%(4). Existen factores geográficos, climáticos, étnicos, alimentarios y genéticos que influyen en la producción y recurrencia de cálculos renales.
Imagenología
El rol de las imágenes es fundamental para el diagnóstico preciso y determinar el tratamiento correspondiente. Permite informar ubicación, tamaño, relación con otros órganos y sospechar complicaciones. Además permite determinar fragilidad del cálculo y actualmente determinar la composición(5).
El 90% de los cálculos de la vía urinaria son radioopacos, siendo la gran mayoría compuestos por oxalato de calcio (80%). Cálculos de acido úrico y de cistina (5-10% y 1-3% respectivamente), pueden ser radiolúcidos a la radiología tradicional, y pueden tener distinto enfrentamiento terapéutico(6).
Radiografia renal y vesical simple y pielografía de eliminación
La radiografía renal y vesical simple históricamente fue el examen inicial para la sospecha de cálculos urinarios, sin embargo presenta una sensibilidad baja menor al 60% para la detección de cálculos. Su principal utilidad actual es la planificación de LEC guiada por fluoroscopía y para la monitorización de fragmentos después de LEC, PNL o ureteroscopía(7).
La pielografía o urografía de eliminación, usa medio de contraste yodado endovenoso excretado por la vía urinaria. Permite mejor evaluación de la anatomía renal y de la vía urinaria, y puede mostrar la presencia de litiasis obstructiva(6). Sin embargo, falla en la detección de cálculos en 31-48% de los casos. En la actualidad el uso de tomosínteisis digital, que corresponde a una serie de radiografías de baja dosis tomadas durante un barrido único del tubo de rayos X en un rango limitado, permite mejorar la detección de cálculos pequeños con radiología convencional(4), y mejorar la calidad diagnóstica de la pielografía de eliminación, manteniendo un bajo nivel de dosis de radiación al paciente.
Ecografía
La ecografía es el método de estudio inicial de elección en pacientes pediátricos y embarazadas, ya que no usa radiación ionizante. Tiene una alta sensibilidad en el diagnóstico de nefrolitiasis, sin embargo, baja su rendimiento en la visualización de cálculos ureterales distales(8). Los cálculos son ecogénicos y presentan sombra acústica posterior, independiente de su composición, y se pueden detectar cálculos menores a 1mm usando este método(6). Existen reportes de que el rendimiento diagnóstico de la ecografía en usuarios expertos es comparable a la tomografía computada (TC).
Las mejoras en el rendimiento de la ecografía, usando equipos modernos y protocolos estrictos de preparación del paciente, han hecho plantear la posibilidad de protocolos de estudio combinando ultrasonografía y radiología convencional en el estudio inicial, bajando levemente la sensibilidad en comparación con TC, pero tomando en consideración la creciente preocupación por la dosis de radiación acumulada de los pacientes(6).
Tomografía computada multidetector
La tomografía computada multidetector de abdomen y pelvis no contrastada (PieloTAC), se ha convertido en el estándar en el estudio de imágenes en contexto de sospecha de cólico renal. Actualmente los protocolos de baja dosis han logrado disminuir el riesgo de la radiación, bajando la dosis efectiva a cifras menores a 5 mSv. Los resultados según metaanálisis demuestran un excelente rendimiento diagnóstico con sensibilidad y especificad de 97% y 95% respectivamente(9). La adquisición de alta resolución se reconstruye en cortes finos de entre 1-3mm, además permite obtener un voxel isotrópico y realizar reconstrucciones volumétricas coronales de alta resolución que mejoran aun más el rendimiento del estudio.
Los lugares más frecuentes donde se puede obstaculizar el avance de los cálculos son la unión pieloureteral, el cruce con los vasos iliacos y la unión ureterovesical, siendo hitos anatómicos a revisar dirigidamente.
Dentro de la información que se debiese reportar en el informe radiológico se encuentran: El número de cálculos; el tamaño mayor en el plano axial en milímetros (medido en ventana ósea), fundamental para establecer probabilidad de expulsión espontánea. La ubicación anatómica en el riñón (superior, medio, inferior), que incide en los resultados de las técnicas de tratamiento y la ubicación anatómica en el uréter (proximal, medio, distal), que se asocia a menor o mayor probabilidad de expulsión. La presencia de signos de obstrucción, infección o de complicaciones como urinomas son de importancia ya que le otorgan urgencia o agresividad al manejo(10).
El uso de medio de contraste yodado solo es de utilidad en la sospecha de complicaciones, en la búsqueda de diagnósticos diferenciales, o especialmente en fase de eliminación cuando existe duda razonable para diferenciar litiasis ureteral distal de flebolito pelviano.
Tomografía computada de doble energía
La composición del cálculo es información fundamental para la definición de tratamientos, principalmente diferenciando cálculos de acido úrico versus no acido úrico (predominantemente de oxalato o fosfato de calcio) debido a que los primeros pueden ser manifestación de un desorden metabólico(5) y son susceptibles a tratamiento médico de alcalinización de orina. Los cálculos de cistina y oxalato de calcio tienen una composición firme que puede limitar el éxito de la LEC(11).
La tomografía computada de doble energía (DECT) adquiere dos sets de datos de baja y alta energía durante una sola adquisición, lo que le confiere una capacidad inherente para diferenciar materiales que tengan similar densidad pero que varían en la absorción de fotones a diferentes niveles energéticos(11). Las dos tecnologías más usadas son la técnica de rápido cambio de voltaje y la técnica de doble fuente de rayos x. Se ha reportado excelente certeza en determinar la composición química de los cálculos renales, determinando su número Z efectivo, con alto grado de concordancia con técnicas in vivo, siendo más confiable que la medición de densidad tomográfica en unidades de Hounsfield (UH), que se realiza con la tomografía computada convencional de energía única. Aún más, se han reportado resultados confiables diferenciando cálculos de acido úrico, cistina, estruvita y oxalato de calcio (Fig 1).
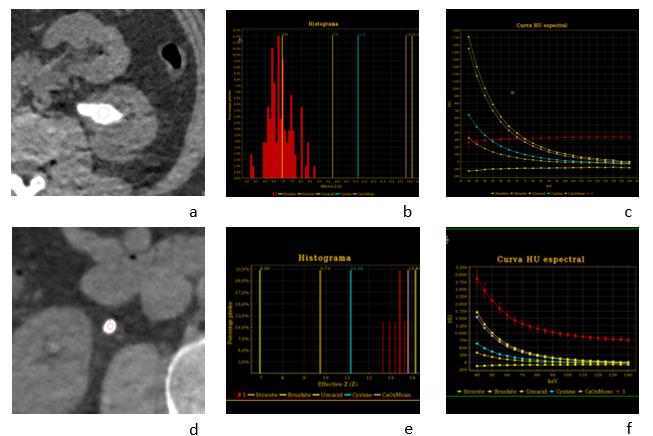

Una limitación es el tamaño del cálculo, ya que el rendimiento baja en cálculos menores de 3mm, en los cuales no es posible realizar una región de interés (ROI) adecuada. Sin embargo, el análisis de estos cálculos no sería de mucha importancia debido a su alta probabilidad de eliminación espontánea.
La litiasis urinaria es un problema de salud creciente, que puede provocar sintomatología con gran disconfort para los pacientes. El advenimiento de nuevas tecnologías en estudios de imágenes ha aumentado considerablemente la certeza diagnóstica en la detección y caracterización de esta patología, disminuyendo los riesgos para los pacientes y permitiendo un tratamiento mejor planificado y más efectivo.
Tumores renales
La incidencia del cáncer renal ha aumentado en las últimas décadas, de 7,1 a 16,4 casos por 100.000 habitantes en Estados Unidos entre 1983 y 2015, con una mortalidad que se mantiene relativamente estable(12). En Chile corresponde al 3% de las neoplasias del adulto, con una incidencia que ha aumentado hasta aproximadamente 4,4 casos por 100.000 habitantes hasta 2012, siendo más común en hombres(13).
Aproximadamente el 20% de las lesiones sólidas renales menores a 4cm son benignas y la mayoría de las lesiones encontradas incidentalmente crecerán lentamente o no tendrán un crecimiento detectable en el tiempo(14). El 90% de los tumores renales malignos son carcinomas de células renales (CCR), el 10% restantes corresponden a tumores mesenquimales, nefroblásticos, metanéfricos, neuroendocrinos, linfoproliferativos y metastásicos(15). El carcinoma urotelial del tracto urinario superior es poco común, correspondiendo al 5-10% de los carcinomas uroteliales.
La ecografía, la tomografía computada (TC), y la resonancia magnética (RM) con sus respectivos avances recientes, son las técnicas más usadas y de mayor utilidad en la detección, diferenciación y clasificación de los tumores renales.
Tumores benignos
Angiomiolipoma
Dentro de las lesiones benignas los angiomiolipomas (AMLs) son los más comunes, correspondiendo en series publicadas hasta el 43% de estas, seguidas por los oncocitomas hasta en 35% de los casos. Los angiomiolipomas son el tumor renal con contenido graso mas frecuente, sin embargo el 5% de los AMLs son pobres en grasa y su diferenciación con RCC en imágenes se hace dificultosa(16). Presentan mayor riesgo de rotura y sangrado cuando miden más de 4cm o si presentan pseudoaneursimas intralesiones prominentes, por lo que pueden ser considerados para embolización o tratamiento quirúrgico. En ecografía son clásicamente hiperecogénicos, sin embargo pequeños CCR también pueden serlo. La detección de grasa macroscópica en TC y RM es la característica imagenológica más específica, con excelente rendimiento en AML clásicos.
Oncocitoma
Los oncitomas son tumores epiteliales benignos, conocidos por simular tanto en imágenes como en patología al subtipo cromofobo de CCR (CCRchr). Son el tumor renal sin grasa mas común, correspondiendo al 7% de las neoplasias corticales renales.
La presencia de una cicatriz central y de hemorragia intratumoral se identifica en el 33% y 20% de los pacientes(14).
Tumores malignos
Carcinoma de células renales (CCR)
Existen varios subtipos histológicos de carcinomas de células renales, los tres más frecuentes son el carcinoma de células claras (CCRcc) que corresponde al 75%, la variante papilar (CCRp) al 7-15% y el 5% al subtipo cromofobo (CCRchr). La sobrevida depende de la etapificación, el grado histológico, presencia de elementos sarcomatoides y de la necrosis(14). Además, cada subtipo tiene características imagenológicas distintas y conllevan un pronóstico distinto, lo que resalta la importancia de diferenciar estas entidades (16).
Carcinoma urotelial
Estos tumores se originan del uroepitelio de cálices y pelvis renal y pueden corresponder hasta el 15% de los tumores renales. Pueden presentar tumores sincrónicos en la vía urinaria en un 24%. La diferenciación con CCR en estadíos iniciales es relativamente fácil, cuando se manifiesta por engrosamiento parietal del tracto urinario o como defecto de llene en el sistema colector. Sin embargo, la presencia de una masa infiltrativa en el seno renal hace más compleja la diferenciación de otras lesiones agresivas.
Linfoma
El escenario más común es la afectación linfomatosa secundaria a linfoma no-Hodgkin. El linfoma renal puede presentarse como masa solitaria simulando CCR, múltiples masas, enfermedad retroperitoneal-perirrenal y como enfermedad renal infiltrativa. El patrón más frecuente es el de múltiples masas, siendo el 60% de los casos. Una lesión solitaria puede presentarse entre el 10% y 20% de los pacientes. Las lesiones tienden a ser de atenuación y señal homogénea en TC y RM respectivamente, con impregnación hipovascular con el contraste endovenoso, lo que las diferencia del CCRcc. La presencia de adenopatías abdominales se da en el 50% de los casos(14).
Escenarios clínicos-imagenológicos
Diferenciación de patología benigna versus maligna
La ecografía presenta capacidad limitada para diferenciar lesiones benignas de malignas. La clásica apariencia hiperecogénica del AML no es específica, y puede presentarse en CCR pequeños (fig 2a).
La detección de grasa macroscópica en una lesión es muy sugerente de AML. En TC se manifiesta como áreas de densidad menor de -10UH. En RM la grasa macroscópica intratumoral presenta intensidad de señal similar a la grasa subcutánea e intraabdominal en todas las secuencias, característicamente con saturación de señal en secuencias de saturación grasa y con artefacto de tinta china en la interfaz agua-grasa periférica en secuencia T1 en fase opuesta. Algunos AML son pobres en grasa y no muestran grasa macroscópica en estudios de imágenes. Estos AML pobres en grasa pueden ser hipointensos en secuencia T2 al igual que los CCRp. Un patrón de impregnación hipervascular intenso favorece el diagnóstico de AML.
Por otro lado, la presencia de necrosis y áreas de hemorragia en una masa renal son sugerentes de CCR y no de lesiones benignas(17).
La diferenciación entre lesiones quísticas y sólidas tiene buen rendimiento en ecografía, TC y RM. La presencia de vascularización al doppler color o poder, o la evidencia de impregnación con contraste endovenoso son hallazgos patognomónicos de lesiones sólidas. En ocasiones es difícil hacer esta definición debido a la presencia de pseudorealce en TC o por la naturaleza hipovascular de la lesión. La TCMD de doble energía (DECT) permite, mediante separación de materiales, realizar mapas de yodo, y así mostrar de manera certera solo las estructuras que captan contraste (Fig. 2b y 2c). La RM mediante técnica de sustracción de fases también permite reconocer estructuras o lesiones que captan contraste (Fig. 2d).
La cuantificación de restricción a la movilidad de protones en secuencia de difusión (DWI) puede potencialmente ser de ayuda para diferenciar lesiones benignas de malignas. Se reportan valores de ADC significativamente menores para CCR que para lesiones benignas (Fig. 2e), siendo particularmente significativa la diferencia con los oncocitomas que presentan valores de ADC más altos. Los AML, sin embargo, pueden presentar valores de ADC bajo, incluso menores que los de CCR.
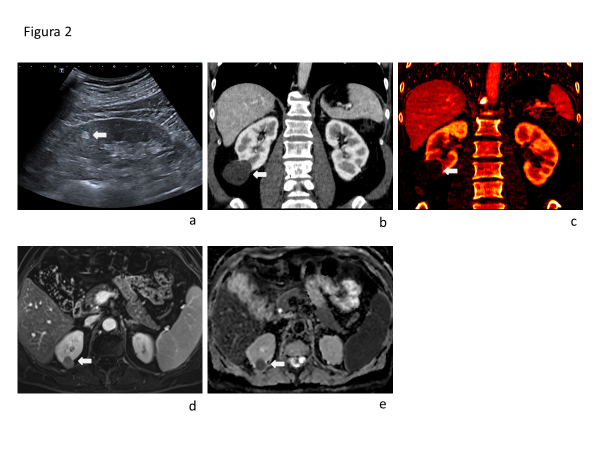

Diferenciación de subtipos de carcinoma de células renales
EL CCRcc presenta impregnación intensa con el contraste endovenoso tanto en TC como en RM en fase cortico medular, con lavado en fase nefrográfica en comparación con el parénquima renal. Los tumores de mayor tamaño son heterogéneos debido a la presencia de necrosis, hemorragia o elementos quísticos (Fig 3a). El CCRp es usualmente mas homogéneo e hipovascular. El patrón de realce dinámico permite diferenciar estas entidades con alta sensibilidad y especificidad(18).
En RM el CCRcc es de alta señal T2, mientras que el CCRp presenta hipointensidad de señal T2 (Fig. 3b). EL 60% de los CCRcc presentan grasa microscópica lo que se identifica por caída de señal en secuencia T1 gradiente en fase opuesta. Los CCRp por su parte pueden contener hemosiderina, lo que se manifiesta como caída de señal en T1 gradiente en fase.
La DECT permite la medición de concentración de yodo intratumoral, y se ha visto que permite distinguir entre CCRcc y CCRp. Usando como punto de corte 0,9mg/ml, se logra un área bajo la curva ROC de 0,92 (IC 95% 0,91-0,93), diferenciando CCRcc con mayor concentración, de CCRp con menor concentración respectivamente(17). Cuando los CCRchr no presentan una cicatriz central estrellada, ni áreas de patrón de realce invertido en secuencias dinámicas, son usualmente indistinguibles imagenológicamente de los CCRcc y de los oncocitomas (Fig. 3c y 3d).
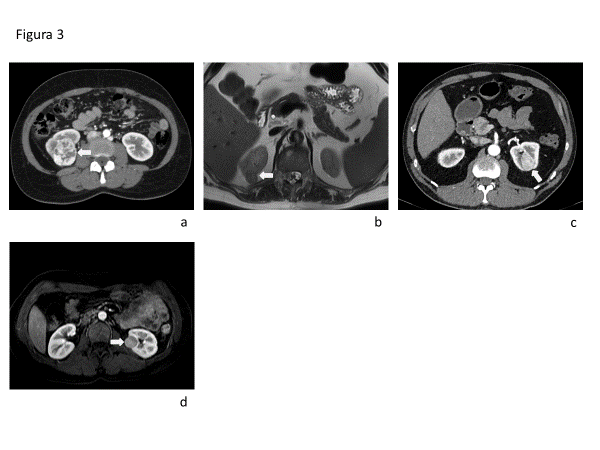

Determinación del grado histológico
El grado tumoral de Fuhrman representa un índice pronóstico de vital importancia en el carcinoma de células renales. Se ha reportado que la cuantificación de concentración de yodo intratumoral usando DECT, tiene correlación significativa con el grado tumoral de Fuhrman, tanto en RCCcc como en RCCp. Así, a mayor concentración de yodo medida, mayor es el grado nuclear de Fuhrman(17).
La restricción en secuencia de difusión (DWI) usando el valor ADC, también se correlaciona con el grado tumoral. A menor valor de ADC (mayor restricción en DWI), mayor el grado tumoral(16).
R.E.N.A.L Score
Las opciones de manejo para lesiones renales pequeñas incluyen nefrectomía parcial, nefrectomía radical, ablación o vigilancia activa, todas siendo opciones razonables dependiendo del escenario clínico. El R.E.N.A.L score es un método estructurado y cuantificable para describir algunas características imagenológicas relevantes, que permitan predecir resultados quirúrgicos.
Se evalúan 5 características: Radio (R), exofítico/endofítico (E), cercanía del tumor al seno renal (N), anterior/posterior (A), y ubicación en relación a líneas polares (L). Se asigna un puntaje de 1 a 3 a todos los descriptores excepto el (A) y se agrupan en 3 grupos, de baja complejidad quirúrgica (4-6 pts), moderada complejidad (7-9 pts) y de alta complejidad (10-12 pts)(19).
Cáncer de próstata
El cáncer de próstata (CP) es una de las principales causas de mortalidad oncológica, representando en Chile la segunda causa de muerte por cáncer en hombres, sólo después del cáncer gástrico.
El diagnóstico del CP difiere de otros cánceres en órganos sólidos, en que el estudio de imágenes se utiliza para identificar pacientes y lesiones que requieren ser biopsiadas. Está basado en biopsia transrectal bajo ultrasonido (TRUS), con muestreo sistemático de la glándula prostática, sin la identificación de una lesión sospechosa. Pacientes elegidos para esta estrategia incluyen aquellos con antígeno prostático específico (APE) elevado y/o tacto rectal alterado en pacientes sin biopsia previa, pacientes de alto riesgo de presentar un cáncer significativo con biopsia previa negativa y hombres con CP de bajo riesgo en vigilancia activa, que requieren repetir la biopsia sistemática para monitorización de la enfermedad(20).
Sin embargo, múltiples causas de elevación del APE no relacionadas a cáncer, errores intrínsecos en el muestreo y la semirandomización de la biopsia (TRUS), y la amplia diversidad genómica como también de pronóstico del CP, conducen a múltiples impactos clínicos y riesgos elevados para los hombres. Entre ellos destacan una importante proporción de pacientes sometidos a TRUS biopsia que no tienen cáncer detectado; biopsias poco fructíferas incurren en un aumento de la morbilidad sin entregar una seguridad completa de ausencia de enfermedad clínicamente significativa. El sobrediagnóstico de cánceres clínicamente no significativos contribuye a ansiedad innecesaria de los pacientes, llevando a sobretratamientos y problemas innerentes, con mínimos beneficios solo para un limitado grupo de pacientes. El subdiagnóstico y subtratamiento de cánceres clínicamente significativos también ocurre debido a problemas en el muestreo en las TRUS biopsia y también en errores en la estratificación, contribuyendo a diagnósticos y tratamientos fallidos, especialmente en pacientes elegidos para vigilancia activa(20,21).
Muchas herramientas están siendo desarrolladas para llegar a diagnósticos más certeros del CP. El paradigma clínico emergente es la utilización de avances imagenológicos y moleculares para el diagnóstico y por ende seleccionar de mejor manera pacientes que requieren biopsia. El desarrollo de la idea de la combinación de métricas de APE (APE, densidad de APE (DAPE), velocidad APE), prostate health index (PHI), score 4K y tests de metilación urinaria del gen de CP, pueden actuar como estimadores de riesgo multivariados para identificar pacientes que pueden presentar un CP clínicamente significativo. Sin embargo, los métodos de selección de pacientes por medio de calculadoras de riesgo no pueden localizar en la glándula prostática CP clínicamente significativos, pudiendo ser perdidos en la TRUS biopsia sistemática. Por lo tanto, el diagnóstico de la biopsia, puede ser incrementado con la utilización de imágenes, especialmente la Resonancia Magnética multiparamétrica (RMmp) en la selección de pacientes y dirigiendo la biopsia a una localización sospechosa, reduciéndose el número de pacientes sometidos a este procedimiento y por consecuencia, sobretratamientos de pacientes con cánceres insignificantes. Es por esto que en el centro de todo esto desarrollo en los últimos años, se encuentra el rol emergente de la RMmp y de la biopsia dirigida por RM para el diagnóstico del CP y la selección del tratamiento(20,21).
Múltiples estudios y experiencia clínica avalan la combinación de RMmp y biopsia dirigida por RM para la detección y localización de CP clínicamente significativos. Ésta estrategia incrementa el diagnóstico de cánceres extensos Gleason score (GS) 3+3 y de intermedio/alto grado (GS 3+4), utilizando menor número de muestras en la biopsia. Esta estrategia ademas disminuye la detección de CP insignificantes(21).
Existen numerosos desafíos en la implementación de la RMmp y de la biopsia dirigida en la práctica clínica, incluyéndose la heterogeneidad en la calidad de las imágenes entre los diferentes centros y por lo tanto variación en el rendimiento en la detección de CP. La calidad de la RMmp de próstata depende de las capacidades que tenga el equipamiento de RM (marca del equipo, campo magnético (1.5T, 3T), gradientes, bobina adecuada, software, hardware, parámetros en las secuencias, factores del paciente (medicación, movimientos, gas rectal, implantes metálicos), hemorragia glandular relacionada a biopsia previa y el factor más importante es la interpretación radiológica de las imágenes (curva de aprendizaje, subjetividad de la observación, variabilidad interobservador y estilo del reporte). Debido a estos desafíos ha sido necesario el desarrollo de estándares de calidad, imágenes y reporte para la RMmp de próstata y estándares de acreditación en el futuro(22).
El año 2012 fue desarrollado el Prostate Imaging-Reporting and Data System (PI-RADS), por un comité conjunto de la American College of Radiology (ACR), European Society of Urogenital Radiology (ESUR) y la AdMeTech Foundation (3,5). Los objetivos del PI-RADS son estandarizar la terminología y contenidos en los reportes de la RMmp, desarrollo de categorías que resuman niveles de sospecha de CP clínicamente significativo (PI-RADS 1- 5), asistencia en la selección de pacientes para biopsia dirigida y manejo, establecer parámetros técnicos aceptables para la realización de la RMmp y reducir la variabilidad en la interpretación(23,24).
La RMmp permite, de manera no invasiva, caracterizar anatómica y funcionalmente la glándula prostática, al usar secuencias morfológicas potenciadas en T2 y complementarla con secuencias funcionales de difusión y perfusión. Sin embargo, es importante destacar que una gran variedad de patología benigna y maligna pueden superponer sus características en la RMmp. Por lo tanto, un score PI-RADS 2, no excluye completamente la posibilidad de un CP clínicamente significativo, pero indica que es poco probable. Del mismo modo un score PI-RADS 5 no es prueba de un CP clínicamente significativo, pero indica que es muy posible(23).
Estudios de correlación histológica entre la prostatectomía-Rmmp han demostrado una mayor visibilidad de lesiones de alto grado y tamaño sin un patrón cribiforme. Una lesión Gleason 3+3 con un patrón de crecimiento sólido necesita un volumen 0.5 ml (aprox. 9-10 mm de diámetro) para ser detectada a diferencia de una lesión índice con un GS 3+4 que necesita un volumen 0.2 ml (aprox. 7-8 mm) especialmente en equipamiento moderno con magnetos de 3T(23).
PI-RADS v2 (2015) y su posterior actualización PI-RADS v2.1 (2019) no apunta a detectar todos los tumores prostáticos, ya que presenta baja sensibilidad para la detección de enfermedad de bajo volumen (<0.5 ml) y CP de bajo riesgo (GS 3+3). Esto permite que la estrategia de RMmp-biopsia dirigida diminuya los sobrediagnósticos y sobretratamientos, como también reduce el número de pacientes sometidos a biopsia que se encuentran en vigilancia activa. Lesiones de alto grado y volumen se detectan con mayor facilidad y presentan categorías de PI-RADS más alto (PI-RADS score 4 y 5) (Figura 4).
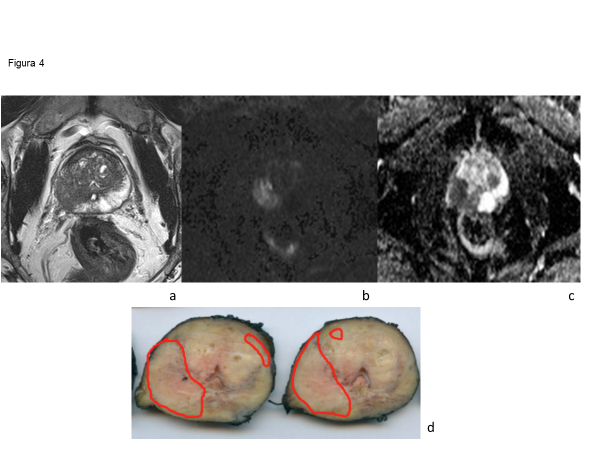

La exactitud del PI-RADS v2 se ha confirmado con revisiones sistemáticas y meta-análisis, demostrándose una sensibilidad de 89% (IC 95% 86-92%) y especificidad 73% (IC 95% 60-83%) para la detección del CP con un valor predictivo negativo (VPN) de entre un 90-95% de acuerdo a los diferentes estudios. En una revisión sistemática de la literatura del PI-RADS v2 y posterior meta-análisis estratificado por Gleason score se demostró una prevalencia de GS 3+4 en lesiones asignadas con score PI-RADS 3 o mayor de aproximadamente un 45%. Se ha demostrado enfermedad clínicamente significativa en lesiones asignadas con scores PI-RADS 1 o 2 (6%), 3 (12%), 4 (48%) y 5 (72%)(23,24).
Cáncer de vejiga
El cáncer de vejiga (CV) es la segunda neoplasia maligna más frecuente del tracto urinario, el cuarto cáncer en hombres y el décimo en mujeres con una relación entre géneros de 4:1. Tiene un peak de incidencia entre 60 y 70 años por lo que se ha considerado clásicamente una enfermedad de personas mayores, sin embargo, la incidencia en pacientes más jóvenes ha ido en aumento y se ha transformado en una de las enfermedades más costosas en su manejo. La gran mayoría de los CV son carcinomas de células uroteliales, clasificándose en cánceres de bajo y alto grado, en músculo invasores (MI) y no músculo invasores (NMI). Los cánceres NMI en general son de bajo grado y por lo general de historia natural indolente(25,26).
El tratamiento del CV tiene como objetivo reducir la recurrencia local y la progresión del estadío de la enfermedad, manteniendo la calidad de vida de los pacientes, bajo una vigilancia estricta para detectar la aparición de invasión muscular. Lesiones de alto grado representan aproximadamente un tercio de los cánceres NMI, sin embargo, pueden progresar a MI y enfermedad metastásica en alrededor de un 20-25% de los pacientes. El éxito del tratamiento depende en el estadío del tumor primario y de la presencia de adenopatías regionales. Se puede llegar a tasas de curabilidad de un 75-80% de los pacientes en enfermedad órgano confinada, de un 60% en estadío T3 con linfonodos negativos y de un 30% con linfonodos positivos(27,28).
El CV en general se diagnostica después de un episodio de hematuria o de síntomas urinarios mixtos, realizándose algún estudio de imágenes (ecografía, tomografía computada, resonancia magnética), confirmándose posteriormente con una cistoscopia flexible. Se realiza una resección transuretral (RTU) del tumor vesical, siendo el tratamiento definitivo de la mayoría de los cánceres NMI y sirve como diagnóstico para la mayoría de los cánceres MI. Una adecuada RTU debe incluir la muscular propia, sin embargo, ocurre subetapificación por pérdida de la infiltración muscular en aproximadamente un 25% de los cánceres invasivos.
La RTU es un método operador dependiente por lo que diferentes tasas de tumor residual se encuentran dependiendo de la experiencia en el procedimiento, lo que refleja resecciones incompletas de tumores vesicales. La re-resección por lo tanto se utiliza en neoplasias de alto grado NMI, previo a quimio-radioterapia por preservación vesical o bien cuando hay diferencias de los hallazgos patológicos y clínicos(28-30).
El rol de las imágenes es fundamentalmente para realizar el diagnóstico de una lesión vesical y también de lesiones sincrónicas en el tracto urinario superior, determinar la presencia de adenopatías regionales y metástasis a distancia(31).
La tomografía computada de abdomen y pelvis con protocolo de urografía (UroTC) es el método de imagen más usado en el estudio de hematuria y en pacientes con diagnóstico de cáncer de vejiga. Las lesiones se pueden presentar como engrosamiento parietal en forma de placa, polipoidea (papilar) o engrosamiento difuso infiltrativo, con reportes de sensibilidad de un 93% y especificidad de un 99. Una de las limitaciones de la TC es la escasa capacidad de diferenciar los diferentes planos de la pared vesical, lo que se traduce en menor certeza en la estadificación local entre 40% y 88%. El rendimiento es menor para estadíos Ta-T2 (77%), y mayor para estadíos T3-T4 (95%). Otra limitación es la incapacidad de diferenciar tumor de edema y fibrosis post tratamiento. La certeza en la detección de extensión extravesical varía entre 40-92%, con baja capacidad de discriminar infiltración neoplásica perivesical de bajo volumen y de diferenciar edema post-tratamiento de infiltración tumoral. La detección de adenopatías metastásicas tiene sensibilidad reportada variable, la cual disminuye de manera importante para micrometástasis. La tomografía computada también da información relevante en cuanto a presencia de metástasis a distancia.
La RMmp de vejiga permite una adecuada estadificación local, ya que es capaz de diferenciar tumores invasores (que invaden músculo detrusor, por lo tanto estadío T2 o superior) de no invasores (T1 o inferior) e identificar la extensión a la grasa perivesical (T3) macroscópica y a órganos adyacentes (T4). Se ha reportado una exactitud de la RM con difusión y contraste intravenoso de hasta un 92% para diferenciar tumores T1 y T2 o mayores(31,32).
Los estudios se pueden realizar tanto en equipos de 1.5T o 3T, con bobina de pelvis de superficie (phased-array) y presencia de vejiga llena. El protocolo óptimo consta de secuencias morfológicas de alta resolución, con una gran capacidad de diferenciar la muscular de una lesión neoplásica como también de la grasa perivesical (secuencias T1 y T2) y secuencias funcionales de difusión y contraste intravenoso con gadolinio, que permiten evaluar el compromiso invasivo de la muscular.
El año 2018 fue desarrollado y publicado el Vesical Imaging-Reporting and Data System (VI-RADS), que busca estandarizar la adquisición y reporte de la Resonancia multiparamétrica (RMmp) de vejiga, definiendo el riesgo de invasión muscular, siendo aplicable a pacientes no tratados y a pacientes con resección transuretral diagnóstica. El sistema de puntuación aplicado va desde VI-RADS score 1 – 5, lo que se traduce en “altamente improbable invasión muscular” a “alta probabilidad de invasión muscular y extravesical” respectivamente. Usando este método se ha reportado un área bajo la curva ROC para invasión muscular de 0,94, con una sensibilidad de 87% y especificidad de 96% para VI-RADS 3 (invasión equivoca o con alta probabilidad)(32).
La utilización de la RMmp ofrece una oportunidad para reducir errores en la estadificación debido a una mejor visualización anatómica de la pared vesical además de ser un método con ausencia de radiación, lo que permite investigar en forma individual a pacientes en riesgo de CV, como también realizar estudio de imágenes previo, durante y en el seguimiento de respuesta a tratamiento (Figura 5).
Finalmente, el PET-CT con FDG tiene su principal uso en la detección de compromiso linfonodal con sensibilidad de 69% y especificidad de 95%, y de metástasis fuera de la pelvis con sensibilidad y especificad de hasta 70% y 94% respectivamente en pacientes con invasión muscular.


De acuerdo a la información de la literatura y nuevos estudios clínicos, se requiere de estudios imagenológicos para la evaluación del compromiso de la pared muscular vesical y diseminación pelviana ya que la estadificación clínica es insuficiente para diferenciar tumores superficiales versus invasores. La etapificación preoperatoria puede ser el factor más importante para el manejo apropiado de estos pacientes.
Medicina nuclear
Las técnicas de imágenes en medicina nuclear se basan en la administración de un trazador radioactivo que, dado su comportamiento en el organismo, permite evaluar una función o una ruta metabólica determinada. Para su uso en urología, tradicionalmente se dispone de varios radiofármacos, dependiendo del órgano o estructura que se desee evaluar. A continuación se describen los exámenes utilizados más frecuentemente.
PET/CT-PSMA
El PET/CT es una técnica híbrida que incluye la evaluación anatómica del cuerpo completo mediante una tomografía computada (CT) y otra funcional mediante la tomografía por emisión de positrones (PET) en un solo estudio. Para la adquisición del PET se requiere la administración de un radiofármaco, en el caso del estudio del cáncer de próstata, un ligando del antígeno específico de membrana prostático (PSMA) marcado con un radioisótopo, los dos disponibles en la actualidad son Ga68 y F18.
El antígeno específico de membrana prostático corresponde a una proteína transmembrana, a pesar de su nombre, no exclusiva de las células prostáticas, con baja expresión en la superficie de las células prostáticas normales y con sobreexpresión en las cancerígenas. Este radiofármaco, Ga68 o F18- PSMA, se acumula en el interior de las células prostáticas neoplásicas lo cual permite su detección tanto en el tumor primario como en las lesiones metastásicas.
Las potenciales utilidades del PET/CT-PSMA son: Evaluación de la recurrencia bioquímica, etapificación de tumores de moderado y alto riesgo y en la evaluación de respuesta a tratamiento.
Recurrencia bioquímica
Las imágenes convencionales tienen una capacidad limitada para detectar recurrencia de enfermedad con niveles bajos de antígeno prostático específico (APE). Existe suficiente evidencia que demuestra la alta sensibilidad del PET/CT-PSMA en la evaluación de recidiva bioquímica, incluso con niveles bajos de APE. La tasa de detección de recurrencia se incrementa a medida que asciende el valor del APE, con tasas de 33% con APE < 0,2 ng/ml y 95% con APE > 2 ng/ml(33).
En un estudio de van Leeuwen PJ et al.(23) , el PET/CT-PSMA demostró alto impacto en el manejo de los pacientes con prostatectomía radical y niveles de APE entre 0,05 y 0,99 ng/ml cambiando el manejo en 29% de ellos (Figura 6).
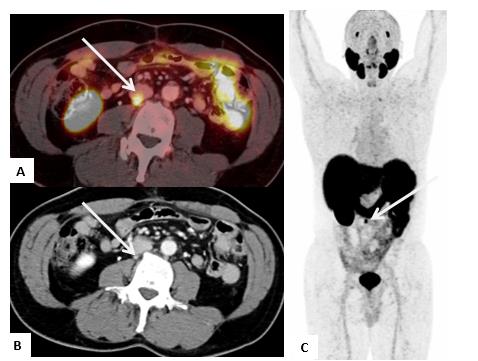

Estadificación
Las guías internacionales no recomiendan el uso del PET/CT-PSMA en la etapificación del cáncer de próstata, sin embargo, existen estudios que han demostrado mayor sensibilidad en la detección de adenopatías metastásicas en comparación a la tomografía computada (TC) en pacientes de riesgo intermedio y alto, con sensibilidad de 66% versus 44% y especificidad de 99% versus 85% respectivamente(35). La menor sensibilidad es debido principalmente a adenopatías secundarias menores de 5 mm.
En relación con la detección de metástasis óseas, un metaanálisis(36) que comparó distintas modalidades de imágenes, entre ellos PET/CT-PSMA y cintigrafía ósea, demostró mayor sensibilidad del PET en la detección, por lesión y por paciente, 88% versus 68% y 97% versus 86% respectivamente, en comparación a la cintigrafía.
El PET/CT-PSMA también es sensible en la detección de metástasis viscerales, las cuales son menos frecuentes (Figura 7).
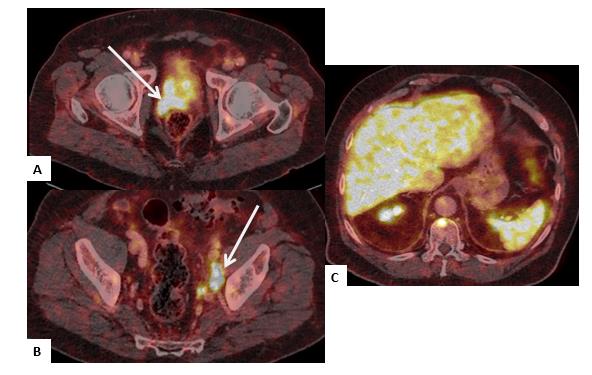

Reestadificación
En la evaluación de la respuesta a tratamiento se recomienda el uso de imágenes convencionales como la TC, cintigrafía ósea o resonancia magnética combinado con los niveles de APE, sin embargo, la cintigrafía ósea detecta actividad osteoblástica y no directamente enfermedad tumoral, por lo tanto, puede confundir lesiones reparativas de verdadera persistencia de enfermedad, no así el PET/CT-PSMA. El PET tiene la ventaja de evaluar la respuesta local, nodal y ósea simultáneamente, sin embargo, no existen estudios suficientes que avalen su uso en la evaluación de respuesta a tratamiento. Una de sus limitaciones potenciales es la ausencia de captación en tumores pobremente diferenciados, como aquellos con diferenciación neuroendocrina, los cuales presentan mayor captación con el trazador fluorodesoxiglucosa (FDG) que con él ligando para PSMA.
Cintigrama óseo
El cintigrama óseo permite la obtención de un mapa de la actividad osteoblástica de todo el esqueleto. Esto se logra mediante la administración endovenosa de un compuesto difosfonado marcado con Tecnecio-99m. Las moléculas que más utilizadas son el metilén-difosfonato (MDP) y el hidroxi-metilén-difosfonato (HMDP), siendo el primero el que por lejos predomina. Luego de la administración del radiofármaco por una vía periférica se espera entre 2 y 4 horas para obtener las imágenes una vez que el trazador se haya fijado en el esqueleto. Estos compuestos se absorben sobre la superficie de los cristales de hidroxiapatita, los cuales se encuentran más expuestos en el hueso de neoformación y más abundante en aquellos sitios en que existe importante recambio óseo, lo que producirá una mayor concentración del trazador radioactivo.
La técnica presenta una alta sensibilidad para la detección de lesiones osteoblásticas, pero una baja especificidad, dado que cualquier patología que genere un mayor recambio óseo provocará una hipercaptación del difosfonato. La alta sensibilidad ha hecho que el cintigrama óseo de cuerpo entero constituya un examen ideal para la detección de metástasis óseas osteoblásticas, como las que ocurren en la mayoría de las lesiones derivadas de un cáncer de próstata.
La probabilidad de compromiso óseo es de menos del 1% en los cánceres con APE<10 ng/ml y ausencia de síntomas de dolor esquelético, y por otro lado es de alrededor de 50% si el APE es >40 ng/ml. Por lo tanto para etapificación inicial se debería solicitar un cintigrama óseo en todo cáncer de próstata con APE>20 ng/ml. El grado de Gleason también se correlaciona con la probabilidad de metástasis en el cintigrama óseo (Gleason menor de 7 v/s Gleason mayor o igual 8) (37,38). En el seguimiento se utiliza el cintigrama óseo para evaluar la presencia de metástasis óseas en caso de elevación de los valores de APE o si aparece dolor óseo sin otra causa que lo explique (39).


Cintigrama renal dinámico
Este examen consiste en la administración endovenosa de un radiofármaco que se excreta por la orina, permitiendo hacer un análisis en el tiempo de su paso por los riñones, uréteres y vejiga. De este modo se obtienen curvas de tiempo v/s actividad y cuantificación de algunos parámetros que permiten evaluar la permeabilidad de la vía urinaria, la eventual presencia de filtraciones (fístulas) y distinguir entre los mecanismos del compromiso de la función renal de un riñón trasplantado (necrosis tubular aguda v/s rechazo)(40).
El radiofármaco de elección es el MAG-3 (mercapto acetil glicina) que se secreta activamente por las células del túbulo contorneado proximal, lo que permite su uso incluso en pacientes con compromiso moderado de la función renal, o en niños con inmadurez renal fisiológica como ocurre en los recién nacidos o prematuros. Como alternativa se puede utilizar DTPA, cuya única ventaja es su menor costo, pero se obtienen resultados que pueden ser menos categóricos cuando la función renal no es totalmente normal. El examen consiste en la administración del trazador por vía endovenosa y adquisición secuencial de imágenes de la región lumbar durante 30 minutos, con controles post miccionales en caso de apreciarse retención del radiofármaco en el sistema excretor. La indicación principal es en pacientes con dilatación de la vía urinaria, congénita o adquirida, en quienes se desee evaluar la presencia de obstrucción funcionalmente significativa en algún nivel (unión pielo-ureteral, urétero-vesical u otro), la evaluación de fístulas urinarias y la monitorización de la evolución de un riñón trasplantado.




Cintigrama renal estático
El cintigrama renal estático consiste en la administración de un trazador que se fija en las células de la corteza renal (específicamente en las células del túbulo contorneado proximal) y permanece casi sin variación durante varias horas, lo cual permite evaluar la morfología y función de cada riñón por separado. El fármaco utilizado es el DMSA , que ha demostrado una alta sensibilidad (95%) para el diagnóstico de lesiones parenquimatosas en la pielonefritis aguda y su seguimiento en el tiempo, ya que aproximadamente 50% de las lesiones visibles en fase aguda revierten al cabo de seis meses y alrededor de 60% al año. Solo aquellos que presentan lesiones en el cintigrama con DMSA en la fase aguda presentarán cicatrices (pielonefritis crónica), en cuyo caso el paciente requiere un control más estricto y el eventual uso de antibióticos profilácticos(41-43). El estudio con DMSA permite también la detección de riñones ectópicos y la cuantificación de la función renal por separado, como puede requerirse en caso de evaluación previo a nefrectomía por distintas situaciones (tumor renal, pielonefritis crónica).



Bibliografía
1. Merenciano F., Escuder A., Manzanero M., Martínez P., ET AL. Significance of simple radiography of the abdomen in nephritic colic. Actas Urol. Esp. 2000; Feb;24(2):138-43.
2. Chan V., Buckley O., Persaud T., Torreggiani W. Urolithiasis: how accurate are plain radiographs? Can Assoc Radiol J. 2008; Jun;59(3):131-4.
3. Coleman J., Nascimento R., Solomon S. Advances in imaging for urologic procedures. Nat. Clin. Pract. Urol. 2007; Sep;4(9):498-504.
4. A. Hesse et al. Study on the prevalence and incidence or urolithiasis in Germany comparing the years 1979 vs 200. Eur Urol, 2003; 44(6), 709-13.
5- J. Dale et al. Imaging Advances in Urolithiasis. Journal of Endourology, 2017; 31, 623-629.
6. P. Cheng et al. What the Radiologist Needs to Know about Urolithiasis: Part 1- Pathogenesis, Types Assessment, and Varian Anatomy. AJR, 2012; 198, 540-547.
7. A. Kambadakone et al. New and Evolving Concepts in the Imaging and Management of Urolithiasis: Urologist´s Perspective. Radiographics, 2010; 30, 603-623.
8.- C. Sandhu et al. Urinary Tract Stones-Part I: Role of Radiological Imaging in Diagnosis and Treatment Planning. Clinical Radiology. 2003; 58, 415-421.
9. T. Niemann. Diagnostic Performance of Low-Dose CT for the Detection of Urolithiasis: A Meta-Analysis. AJR. 2008; 191. 396-401.
10. P. Cheng et al. What the Radiologist Needs to Know about Urolithiasis: Part 2- CT Findings, Reporting, and Treatment. AJR, 2012; 198, 540-547.
11. G. Hidas et al. Determination of Renal Stone Composition with Dual-Energy CT: In Vivo Analysis and Comparison with X-ray Diffraction. Radiology. 2010; 257(2). 394-401.
12. Kidney and Renal Pelvis. American Cancer Society. Cancer Statistics Center. http://cancerstatisticscenter.cancer.org/. December 19, 2019.
13. J. López.Epidemiología del Cáncer Urogenital en Chile. Rev. Med. Clin. Condes. 2018; 29(2). 118-127.
14. F. Kay et al. Imaging of Solid Renal Masses. Radiol Clin N Am. 2017; 55(2). 243-258.
15. H. Moch et al. The 2016 WHO Classification of Tumours of the Urinary System and Male Genital Organs- Part A: Renal, Penile, and Testicular Tumours. Eur Urol. 2016; 70(1). 93-105.
16. T. van Oostenburugge et al. Diagnostic Imaging for Solid Renal Tumors: A Pictorial Review. Kidney Cancer. 2018; 2(2). 79-93.
17. A. Mileto et al. Iodine Quantification to Distinguish Clear Cell Carcinoma at Dual-Energy Multidetector CT: A Multireader Diagnostic Performance. Radiology. 2014; 273(3). 813-820.
18. MRM. Sun et al. Renal Cell Carcinoma: Dynamic Contrast-Enhanced MR Imaging for Differentiation of Tumor Subtypes-Correlation with Pathologic Findings. Radiology. 2009; 250(3). 793-802.
19. D. Canter et al. Utility of the R.E.N.A.L Nephrometry Scoring System in Objectifying Treatment Decision-making of the Enhancing Renal Mass. Urology. 2011; 78(5). 1089-1094.
20. Giganti, F., Rosenkrantz, A. B., Villeirs, G., Panebianco, V., Stabile, A., Emberton, M., & Moore, C. M. (2019). The Evolution of MRI of the Prostate: The Past, the Present, and the Future. AJR. American Journal of Roentgenology, 1–13.
21. Padhani, A. R., Weinreb, J., Rosenkrantz, A. B., Villeirs, G., Turkbey, B., & Barentsz, J. (2019). Prostate Imaging-Reporting and Data System Steering Committee: PI-RADS v2 Status Update and Future Directions. European Urology, 75(3), 385–396.
22. Barentsz, J. O., Weinreb, J. C., Verma, S., Thoeny, H. C., Tempany, C. M., Shtern, F., et al. (2015). Synopsis of the PI-RADS v2 Guidelines for Multiparametric Prostate Magnetic Resonance Imaging and Recommendations for Use. European Urology, 69(1), 1–9.
23. Barkovich, E. J., Shankar, P. R., & Westphalen, A. C. (2019). A Systematic Review of the Existing Prostate Imaging Reporting and Data System Version 2 (PI-RADSv2) Literature and Subset Meta-Analysis of PI-RADSv2 Categories Stratified by Gleason Scores. American Journal of Roentgenology, 212(4), 847–854.
24. Turkbey, B., Rosenkrantz, A. B., Haider, M. A., Padhani, A. R., Villeirs, G., Macura, K. J., et al. (2019). Prostate Imaging Reporting and Data System Version 2.1: 2019 Update of Prostate Imaging Reporting and Data System Version 2. European Urology.
25. Svatek RS, Hollenbeck BK, Holmang S, et al. The economics of bladder cancer: costs and considerations of caring for this disease. Eur Urol 2014;66:253–62.
26.- AntoniS,FerlayJ,SoerjomataramI,ZnaorA,JemalA,BrayF. Bladder cancer incidence and mortality: a global overview and recent trends. Eur Urol 2017;71:96–108.
27. Soukup V, Capoun O, Cohen D, et al. Prognostic performance and reproducibility of the 1973 and 2004/2016 World Health Organization grading classification systems in non-muscle-invasive bladder cancer: a European Association of Urology Non-muscle Invasive Bladder Cancer Guidelines Panel systematic review. Eur Urol 2017;72:801–13.
28. Linton KD, Rosario DJ, Thomas F, et al. Disease specific mortality in patients with low risk bladder cancer and the impact of cystoscopic surveillance. J Urol 2013;189:828–33.
29. Babjuk M, Bohle A, Burger M, et al. EAU guidelines on non-muscle invasive urothelial carcinoma of the bladder: update 2016. Eur Urol 2017;71:447–61.
30. Fonteyne V, Ost P, Bellmunt J, et al. Curative treatment for muscle invasive bladder cancer in elderly patients: a systematic review. Eur Urol 2018;73:40–50.
31. Verma, S., Rajesh, A., Prasad, S. R., Gaitonde, K., Lall, C. G., Mouraviev, V., et al. (2012). Urinary bladder cancer: role of MR imaging. RadioGraphics, 32(2), 371–387.
32. Panebianco, V., Narumi, Y., Altun, E., Bochner, B. H., Efstathiou, J. A., Hafeez, S., et al. (2018). Multiparametric Magnetic Resonance Imaging for Bladder Cancer: Development of VI-RADS (Vesical Imaging-Reporting And Data System). European Urology, 74(3), 294–306.
33. Perera M, Papa N, Roberts M, Williams M, Udovicich C, Vela I, et al. Gallium-68 Prostate-specific Membrane Antigen Positron Emission Tomography in Advanced Prostate Cancer—Updated Diagnostic Utility, Sensitivity, Specificity, and Distribution of Prostate-specific Membrane Antigen-avid Lesions: A Systematic Review and Meta-analysis. European Urology. 2019 Feb.
34. van Leeuwen PJ, Stricker P, Hruby G, Kneebone A, Ting F, Thompson B, et al. 68 Ga-PSMA has a high detection rate of prostate cancer recurrence outside the prostatic fossa in patients being considered for salvage radiation treatment. BJU Int. 2016 May;117(5):732–9.
35. Maurer T, Gschwend JE, Rauscher I, Souvatzoglou M, Haller B, Weirich G, et al. Diagnostic Efficacy of 68 Gallium-PSMA Positron Emission Tomography Compared to Conventional Imaging for Lymph Node Staging of 130 Consecutive Patients with Intermediate to High Risk Prostate Cancer. Journal of Urology. 2016 May;195(5):1436–43.
36. Zhou J, Gou Z, Wu R, Yuan Y, Yu G, Zhao Y. Comparison of PSMA-PET/CT, choline-PET/CT, NaF-PET/CT, MRI, and bone scintigraphy in the diagnosis of bone metastases in patients with prostate cancer: a systematic review and meta-analysis. Skeletal Radiol. 2019 May 24.
37. Oyen W., Witjes J., Corstens F. Nuclear medicine techniques for the diagnosis and therapy of prostate carcinoma. Eur Urol. 2001 Sep; 40(3):294-9.
38. Jaukovic L., Adjinovic B., Cerovic S., Joksimovic M., et al. Is bone scintigraphy necessary in initial staging of prostate cancer patients? Hell J Nucl Med. 2011 May-Aug;14(2):126-30.
39. Jana S., Blaufox M. Nuclear medicine studies of the prostate, testes, and bladder. Semin Nucl Med. 2006 Jan;36(1):51-72.
40.-Sfakianaki E., Sfakianakis G., Georgiou M., Hsiao B. Renal scintigraphy in the acute care setting. Semin Nucl Med. 2013 Mar;43(2):114-28. doi: 10.1053/j.semnuclmed.2013.01.001
41.-Rushton H., Majd M. Dimercaptosuccinic acid renal scintigraphy for the evaluation of pyelonephritis and scarring: a review of experimental and clinical studies. J Urol 1992 Nov;148(5 Pt 2):1726-32.
42. Hitzel A., Liard A., Véra P., Manrique A., et al. Color and power Doppler sonography versus DMSA scintigraphy in acute pyelonephritis and in prediction of renal scarring. J Nucl Med 2002 Jan; 43:27–32.
43. Donoso R., Lobo S., Arnello V., Arteaga M., et al. Renal scars after one year of follow up in children with a first episode of acute pyelonephritis. Rev Méd Chile 2006; 134: 305-311.
